Уважаемые друзья, мы продолжаем цикл статей, посвященных «наращиванию костной ткани» или, проще говоря, остеопластике и остеопластическим операциям. Чтобы быстро войти в курс дела, рекомендуем ознакомиться с предыдущими частями:
Часть I. Что такое остеопластика и для чего она вообще нужна?
Часть II. Какие существуют методы наращивания костной ткани и чем они отличаются между собой.
А сегодня я предлагаю вам, дорогие друзья, поговорить о биоматериалах. То, что мы все называем «искусственной костью», «заменителем костной ткани», «мембраной», «искусственной слизистой оболочкой» и т. д. Вот вы приходите к доктору на консультацию по остеопластике и слышите:
— Вот тут мы подсыпем косточку, потом накроем барьерной мембраночкой, постучим молоточком — так и делается наращивание челюстной кости!
Признаюсь честно, если бы мне на консультации имплантолога такое сказали — сбежал бы нафиг. Чуть позже, вы поймете, почему.
Итак, на повестке дня следующие темы:
Вместо пролога. Что такое биоматериалы?
«Искусственная костная ткань» — такая ли уж она искусственная?
Барьерная мембрана — самый непонятный предмет. Вроде, он есть, но через три месяца уже нет.
«Искусственная слизистая» — новое слово в регенеративной хирургии и имплантологии.
Мы обсудим каждый из этих, используемых в имплантологической практике, биоматериалов, рассмотрим происхождение, свойства, попытаемся понять принципы и необходимость использования.
И, в конце концов, я попытаюсь ответить на самый главный вопрос:
Какие биоматериалы самые лучшие?
Если вас волнует только последнее — смело мотайте в самый конец статьи, не забивайте себе голову всякой ерундой.
Вместо пролога. Что такое биоматериалы?
С точки зрения толкового словаря, под биоматериалами подразумеваются любые чужеродные вещества и объекты, внедряемые в организм и дополняемые его структурно или/и функционально, и использующиеся в медицинских целях. То есть, биоматериалами можно назвать искусственные клапаны сердца, эндопротезы, имплантаты, в т. ч. дентальные, металлоконструкции, применяемые при остеосинтезе, гемостатические средства, зубные протезы, коронки, вкладки, пломбы и т. д. И наоборот, сережки для пирсинга, краски для татуировок, всякие страшные штуки для боди-моддинга к биоматериалам, в правильном их понимании, не относятся.
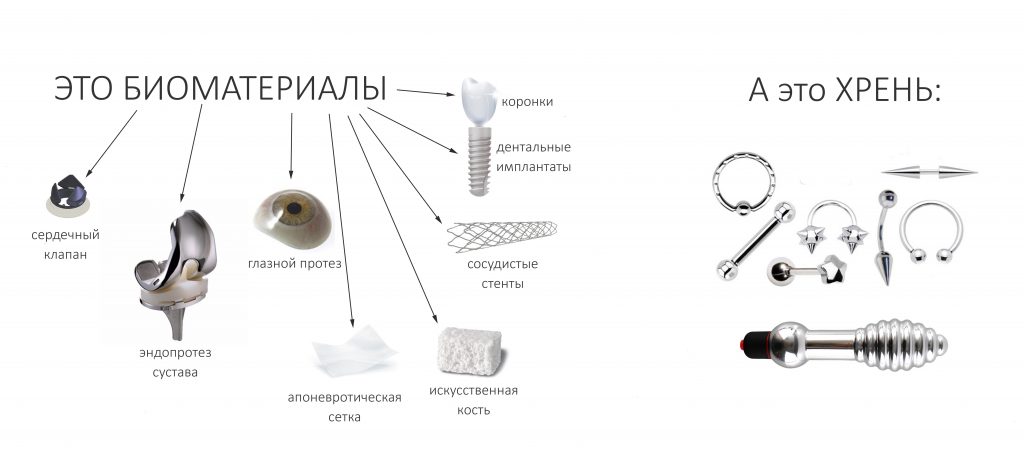
То, что мы используем для «наращивания костной ткани», было бы правильнее назвать «биоматериалами для регенеративной хирургии», что конкретизирует и объясняет их назначение. В общих чертах, современный стоматологический рынок предлагает нам три категории таких материалов — остеографты, барьерные мембраны и мукографты:
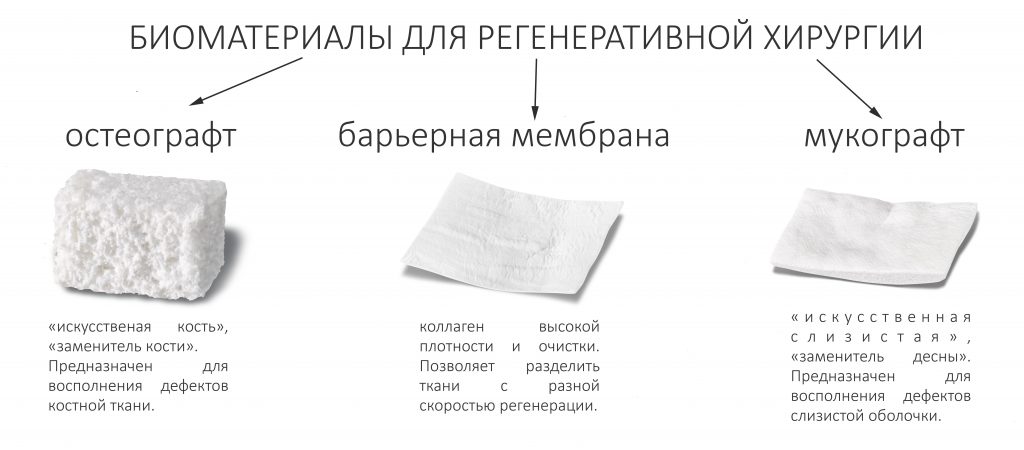
Чуть позже, мы подробно рассмотрим каждую из этих категорий.
Говорить о показаниях и противопоказаниях к использованию биоматериалов с точки зрения пациента достаточно сложно, поэтому их использование в ходе тех или иных остеопластических операций — вопрос, относящийся больше к конкретной методике, нежели к самому материалу. Поэтому мы будем рассматривать его в статьях, посвященных определенным методикам остеопластики. То есть, скоро.
Но, в целом, уважаемые друзья, вам нужно знать следующее:
— использование биоматериалов — это всегда компромисс, вынужденная мера.
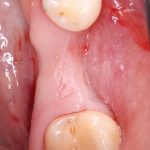
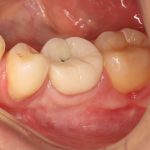
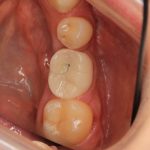
Да, теоретически и практически, мы могли бы обходиться без них. И тому есть масса примеров:
уточню, что на двух правых снимках — временная коронка на установленном имплантате. Биоматериалы для остеопластики в данном клиническом случае не применялись.
Но в таких случаях мы сталкиваемся с проблемой — если нам необходимо возместить атрофическую утрату кости или слизистой оболочки, то её необходимо где-то взять. И нередко процесс получения аутотрансплантата (т. е., собственного фрагмента тканей для пересадки) увеличивает травматичность, сложность и продолжительность хирургического вмешательства. А иногда вообще является отдельной хирургической операцией со всеми вытекающими: повышаются риски осложнений и снижается безопасность хирургического лечения. Совершенно логичным выглядит желание всего этого избежать, заменив аутотрансплантат чем-то «искусственным».
— ни один из существующих биоматериалов не улучшает качество регенерирующих тканей.
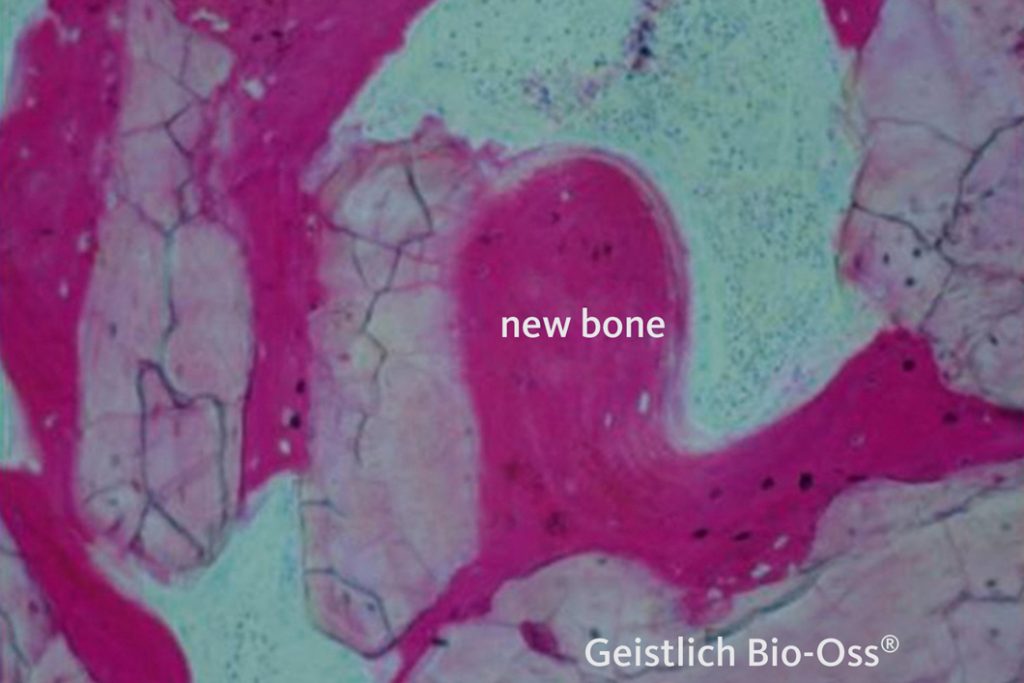
Это микроскопная фотография того, что получается после остеопластики с использованием биоматериалов.
Если мы говорим, к примеру, о «наращивании костной ткани», то ни один из остеографтов, используемых в современной хирургической практике, не делает кость крепче, прочнее, красивее и т. д. Более того, то, что мы получаем в результате использования «искусственных заменителей кости», сложно назвать костью в биологическом смысле — скорее, это костная мозоль с включением частиц биоматериала(как на микроскопной картинке выше), её свойства и структура сильно отличаются от нормальной здоровой костной ткани. Если уж говорить совсем серьезно, то использование графтов «ухудшает» качество тканей. Но мы вынуждены идти на этот компромисс, чтобы восполнить их объем и, соответственно, создать условия для нормальной имплантологической реабилитации.
— не существует биоматериалов, ускоряющих регенерацию тканей.
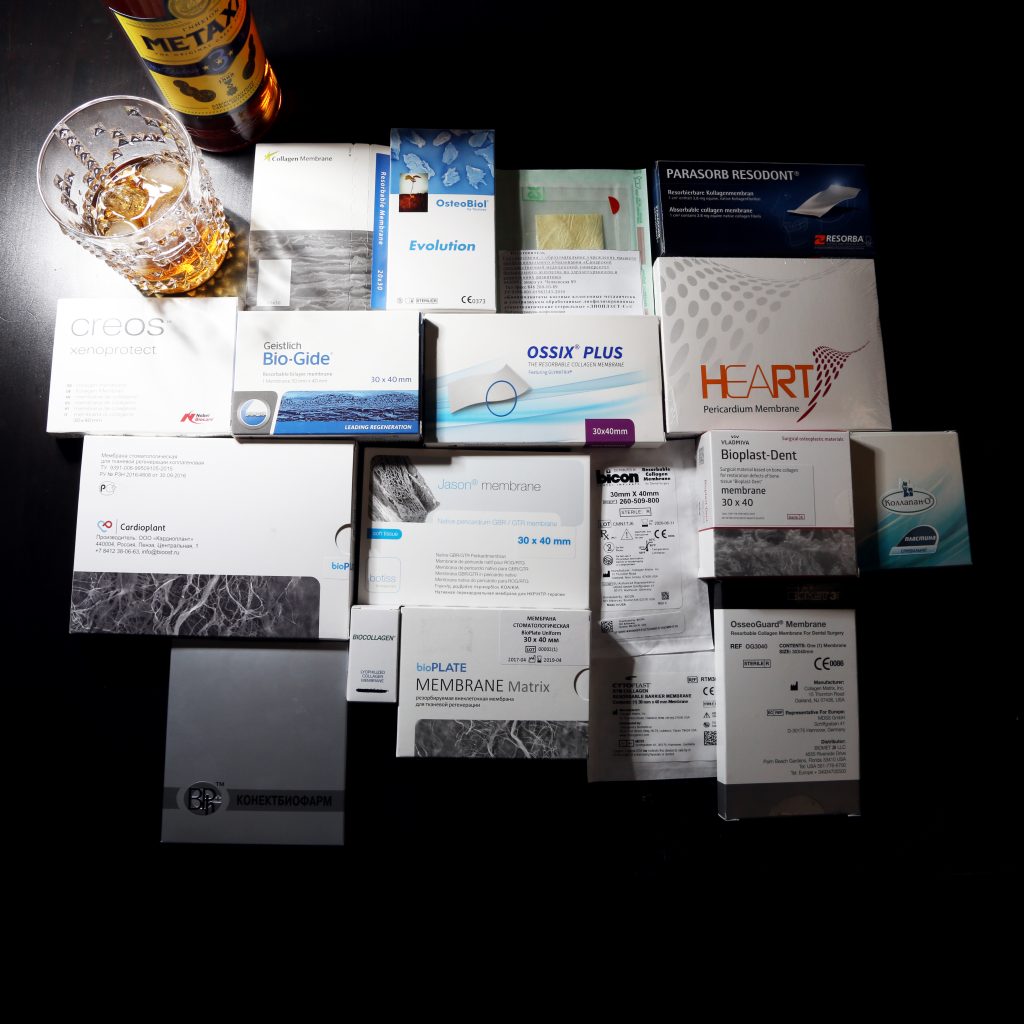
Я бы даже сказал больше — от марки, производителя или страны происхождения биоматериала мало, что зависит. Все существующие в мире графты и барьерные мембраны работают одинаково, по одним и тем же биологическим законам. Категорически неправильно утверждать, что «этот материал работает лучше, чем этот» или «вот этот хороший, а этот — полное говно!». Безусловно, биоматериалы отличаются между собой целым рядом свойств, и сегодня мы с вами обязательно поговорим об этих свойствах.
— у каждой из категорий биоматериалов есть своё назначение и чётко прописанная функция.
Прямо как на этой картинке:
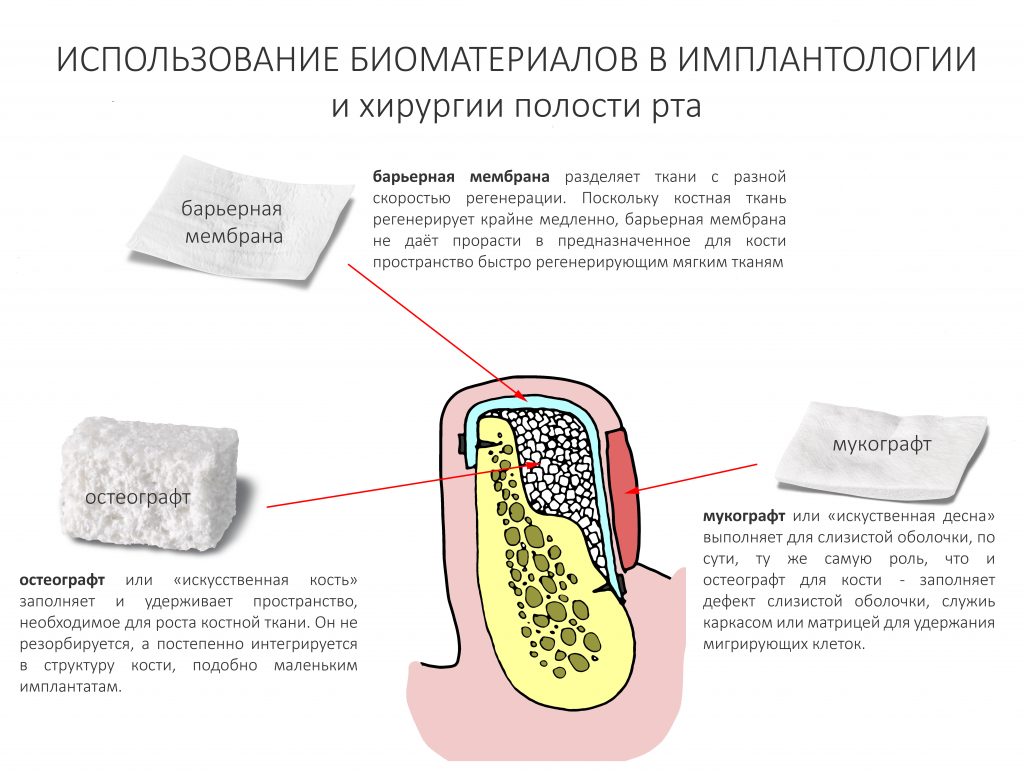
Использовать биоматериалы не по назначению — это, как минимум, серьезно рисковать результатом. Например, мы можем попытаться с использовать гемостатическую губку для заполнения субантрального пространства при синуслифтинге. И, возможно, мы даже получим хороший результат. Но, только слово «возможно» меня лично очень смущает. В хирургии использование этого слова должно быть сведено к минимуму.
— использование биоматериалов должно быть обоснованным и понятным, прежде всего, вам.

«Сюда засунем, здесь приколотим» … иными словами, использование графтов и барьерных мембран, — это всегда отличный способ завысить стоимость лечения или искусственно усложнить предстоящую операцию. И действительно, установленные имплантаты можно пересчитать, по контрольным снимкам легко определяется их марка и модель, а вот определить объем де-факто использованного при синуслифтинге графта или размер установленной барьерной мембраны (да и вообще, наличие этой самой мембраны) не так уж и просто. Если вы по каким-то причинам не понимаете, для чего необходимо использование биоматериалов в вашем клиническом случае, значит, они не нужны. Об их применении в различных клинических ситуациях мы поговорим в последующих статьях, когда будем изучать каждый из существующих методов остеопластики. Ну и, после операции имеет смысл «свериться» с реальным расходом биоматериалов — все графты и барьерные мембраны используемые в современной хирургии, имеют специальные наклейки с указанием их параметров и серийных номеров, — одна наклейка остаётся в медицинской карте, вторая вклеивается в договор, на контрольный снимок или специальный бланк, которые передаются пациенту.

Наконец, последнее, от того не менее важное:
все существующие биоматериалы — одноразовые. Одна упаковка предназначена ТОЛЬКО для одной операции:

Это, собственно, значит, что во-первых, неиспользованные остатки биоматериалов нельзя повторно стерилизовать и использовать, а во-вторых, что отсутствие вышеуказанной наклейки говорит о том, что в вашем лечении, возможно, был использован «левый» материал или остатки с какой-то другой операции. Категорически не рекомендую на этом экономить, ибо правильно простерилизовать уже открытый материал в условиях обычной стоматологической клиники без потери его свойств невозможно.
В принципе, уважаемые друзья, знания вышеперечисленного вполне достаточно, чтобы понять, нужны ли недешевые, в общем-то, биоматериалы для наращивания костной ткани конкретно в вашем клиническом случае. На всякий случай напоминаю, что
если вы чего-то не понимаете, — значит вам это не нужно.
Вспомните, хотя бы, вот эту статью>>.
В рамках семинаров RegenerationDay by Geistlich, мне удаётся не только повысить чувство собственной важности, но и побеседовать с докторами из различных клиник, городов и регионов нашей страны. И я не могу не замечать зловредную тенденцию — чрезмерное злоупотребление биоматериалами, бестолковое желание затолкать их туда, где они, в принципе, не нужны. Многие в них видят какую-то панацею, некую «волшебную таблетку», способную, если не гарантировать, то улучшить результат любой остеопластической операции. Увы, это не так.
В нашем стоматологическом центре делается очень много остеопластических операций — больше двухсот с начала года. При этом, расход биоматериалов относительно небольшой — они используются меньше, чем в половине случаев. Почему? Для ответа на этот вопрос нужно, как минимум, прочитать вот это>> или просто заглянуть к нам в клинику на консультацию.))
«Искусственная костная ткань» — такая ли уж она искусственная?
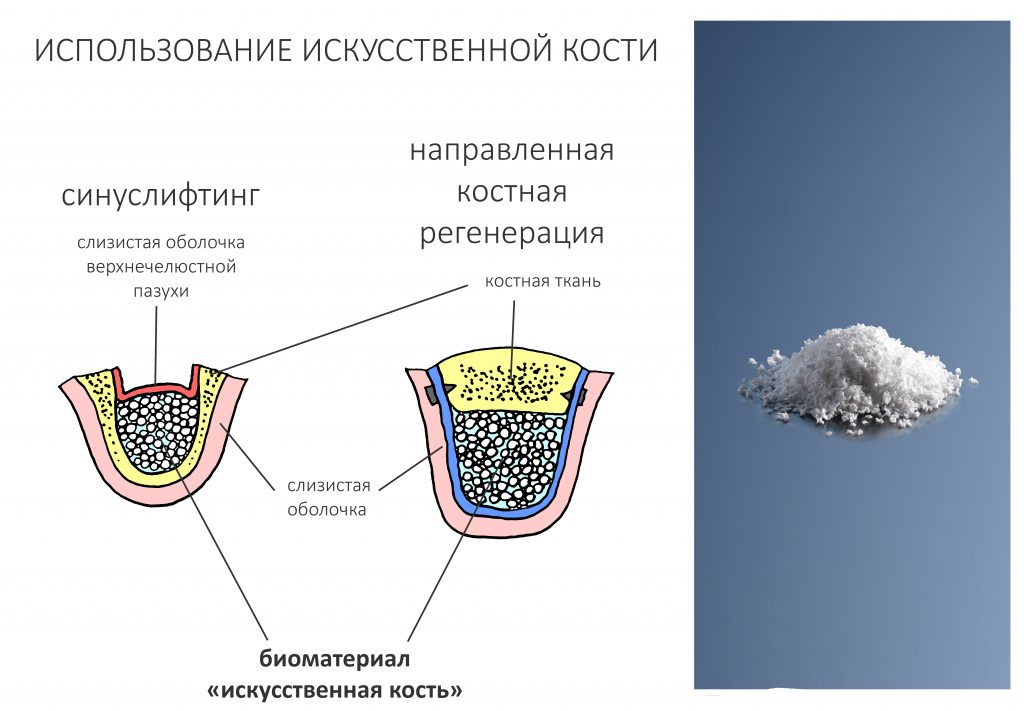
У простого обывателя, не связанного с медициной, имплантологические биоматериалы ассоциируются, чаще всего, именно с «заменителем костной ткани» или, как её еще называют в народе «костным порошком» или «искусственной костью». По мнению многих, у данной категории биоматериалов наиболее понятное и простое применение — заполнить место, где не хватает кости — и там сразу вырастет костная ткань.
На практике, всё получается немного сложнее.
Источники
По происхождению, остеографты (это правильное название данной категории биоматериалов) можно разделить на три группы:
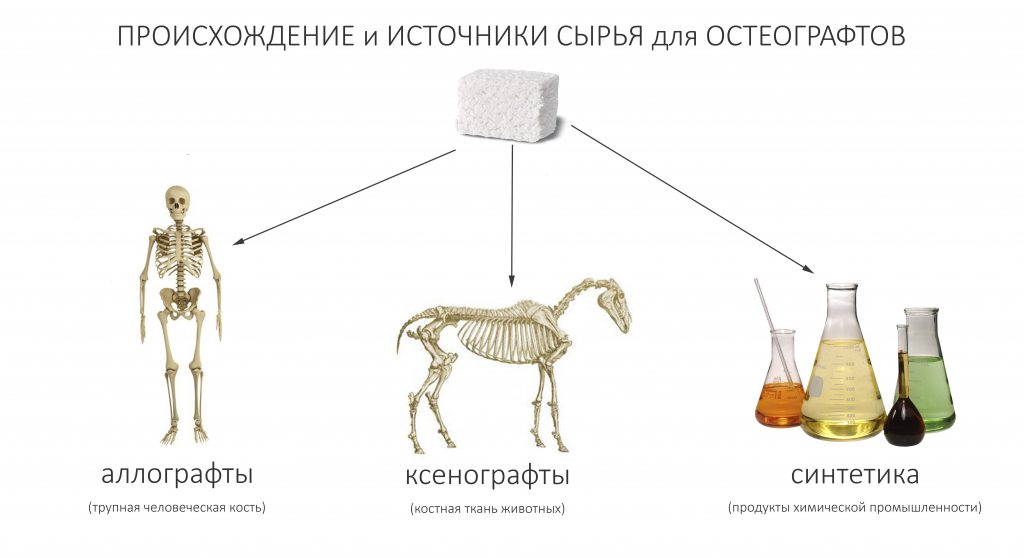
Аллографты — трупная (человеческая) костная ткань, обработанная специальным образом. Их доля в современной имплантологической практике относительно невысока. На то есть целый ряд причин: трудности в поиске и подборе источников сырья, связанные с этим морально-этические дилеммы, техническая сложность и длительное время обработки, законодательные ограничения в ряде стран и т. д.
Примерами аллографтов могут служить материалы Alloplant, Allograft, MAP3, NovaBone и др.
Синтетические графты изготавливаются химическим способом и представляют из себя, как правило, структурно однородное вещество с конкретной химической формулой. Чаще всего, это какой-нибудь трикальцийфосфат или гидроксиапатит.Хотя, изредка встречаются и различные кальциты-флюориты, вплоть до кварцевого песка. Производство синтетических графтов относительно простое, нет необходимости париться с обработкой и удалением антигенов, поэтому они — самые дешевые на стоматологическом рынке. И, наверное, именно синтетика в полной мере отвечает термину «искусственная костная ткань», поскольку именно она производится из неорганического сырья, в то время как алло- и ксенографты, всё же, имеют натуральное происхождение.
Примерами синтетических остеопластических материалов являются Изиграфт, КроноОсс, BoneCeramic, BioGrain и т. д.
Ксенографты — обработанная специальным образом костная ткань животного происхождения. Источником для неё служит крупный и мелкий рогатый и нерогатый скот, вплоть мелких домашних животных и хомячков. На сегодняшний день — это самый распространенный и востребованный вид остеографтов. Поскольку, с одной стороны, во-первых, в структуре костной ткани человека и животных нет какой-то принципиальной разницы, а во-вторых, риски при их использовании гораздо ниже, чем у аллографтов. Существенный плюс — это почти полное отсутствие морально-этических, законодательных и сертификационных проблем, связанных с получением, обработкой и использованием ксенографтов.
Типичными примерами ксенографтов являются Bio-Oss, Cerabone, MP3, Endobone и многие-многие другие.
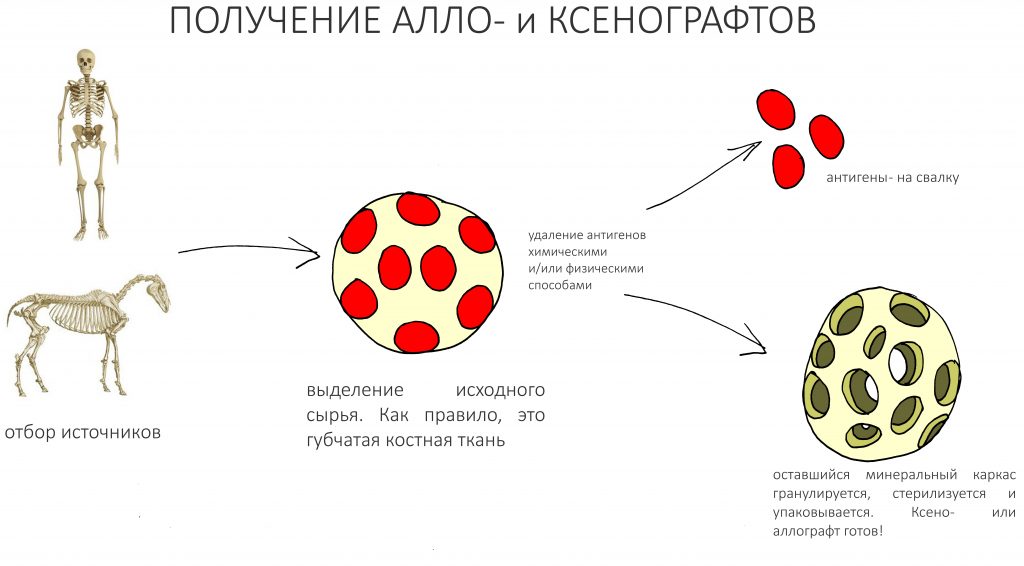
Получение и обработка.
Главное свойство всех графтов, биосовместимость, достигается путём удаления антигенов, специальных молекул-маркеров, по которым организм разделяет все попадающие в него объекты на «своё» и «чужое».
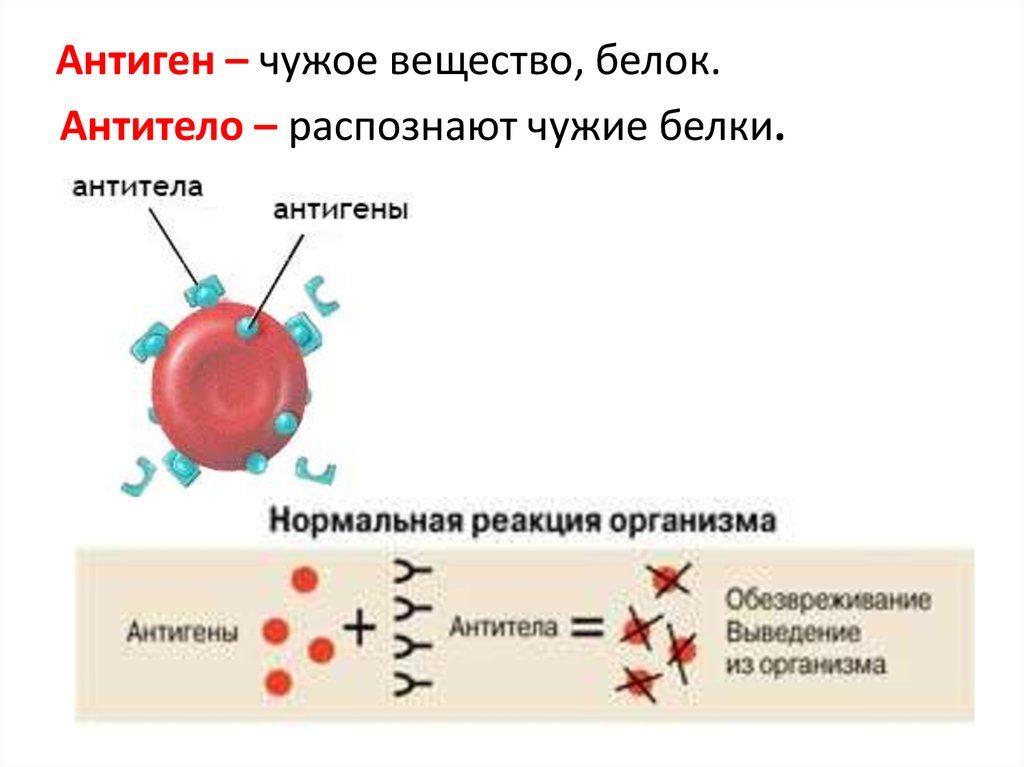
С синтетикой тут проще всего, она изначально лишена антигенов. Если молекула SiO2 (кварц), трикальцийфосфата или гидроксиапатита Ca10(PO4)6(OH)2 не имеет маркеров и биологически нейтральна для организма, то графт из такого материала будет также биологически нейтрален. Всё, что нам нужно — это найти способ получения химически чистого вещества, придать ему какую-нибудь форму («форм-фактор», см. ниже) — и всё на этом. Осталось простерилизовать, запаковать — и можно продавать по 1000 рублей за кг — имплантологи оценят!

С ксенографтами всё сложнее. Антигены — это, прежде всего, органические молекулы, поэтому из хорошего графта удаляется вся побочная органика, оставляется только минеральный матрикс. Принципиально важно сохранить структуру костной ткани, иначе всё преимущество ксенографтов пропадает — и это, я замечу, наиболее сложный технологический этап производства. Так получают минеральные неорганические матриксы. При необходимости, в них добавляют коллаген — так получают коллаген-содержащие графты. Я должен заметить, что коллаген в таких случаях используется «левый», т. е. источник его происхождения иной, нежели минеральный матрикс. Такие коллаген-содержащие биоматериалы — редкость, почти 99% рынка остеографтов — это чистая минералка.
С аллографтами — так вообще технологический ужас. Если не удалённые антигены животного происхождения, чаще всего, приводят к соответствующей реакции в виде воспаления/отторжения, то человеческая органика, оставшаяся из-за недостаточной обработки графта, плюс к этому, способна вызывать или спровоцировать ряд серьезных заболеваний (гуглите аутоимунные и прионные заболевания).
Поэтому получение и обработка этих биоматериалов, по идее, должна быть гораздо более строгая, тщательная и долгая. Не говоря уже о сложностях в отборе сырья. Как правило, по этим причинам аллографты стоят дороже ксенографтов.
Что ВАЖНО и на что НАПЛЕВАТЬ при выборе остеографта для работы?
Для начала, избавлю всех вас от иллюзий и еще раз подчеркну, что все существующие марки «искусственной кости» работают по одним и тем же принципам, и с любым из легально присутствующих на рынке остеографтов можно получить хороший результат остеопластической операции. Если вам, дорогие друзья, пытаются втереть, что «вот этот костный материал лучше работает, чем этот, но он дороже» — вас, мягко говоря, разводят, пользуясь вашей некомпетентностью.
Добавлю еще, что вы никогда не узнаете и не сможете проверить, использовал ли доктор тот материал, за который вы заплатили. Увы, но тут всё зависит лишь от того, насколько врач дорожит своей репутацией. Поэтому не обращайте на марку и страну происхождения биоматериала, поскольку они не имеют никакого значения для успеха вашего имплантологического лечения. Всё, что вам нужно для результата — это доктор, которому вы доверяете. Ну и, который имеет соответствующие условия для вашего лечения.
А теперь поговорим о том, что действительно важно. Чем же костные материалы различаются между собой?
1. Форм-фактор.
Простым языком, это форма выпуска. То как выглядит биоматериал. Остеографт может выпускаться в виде цельного костного фрагмента, пластин или блоков, гранул, небольших кусочков, порошка и т. д. Он может быть упакован в специальный аппликатор, находиться в блистере или банке.

Ну и, сами частицы графта могут быть разных размеров. При одинаковом весе, это будет влиять на объем. Например, привычная всем упаковка Geistlich Bio-Oss S весом 0,5 г имеет объём, приблизительно, 1 куб. см, а большие по размеру гранулы Geistlich Bio-Oss L того же веса будут занимать объём 1,5 куб. см. Это значит, что крупными гранулами можно заполнить объем на треть больше (напомню, что упаковки L и S стоят одинаково).

Кроме того, он может быть однофазным (т. е., состоять только из сухого твердого вещества), а может быть двухфазным, предварительно смоченным каким-то раствором и готовым к работе. В целом, существует огромное количество видов упаковок остеографтов, фактически, для любого клинического случая.
Безусловно, мы будем выбирать тот форм-фактор нашего остеографта, который максимально подходит для нашей работы. Скажем, для синуслифтинга удобнее, практичнее и правильнее использовать остеографт в виде гранул, упакованный специальный аппликатор. И наоборот, для остеотомии мы будем использовать остеографт в виде блока — им проще удержать «расщепленные» фрагменты на месте, иногда для них даже не требуется специальной фиксации.
2. Физические и биологические свойства
Уважаемые друзья, будучи пациентами, у вас вряд ли будет возможность изучить физические и биологические свойства остеографтов, столь важные для нашей работы. Тем не менее, я попробую представить их в виде общей картинки:
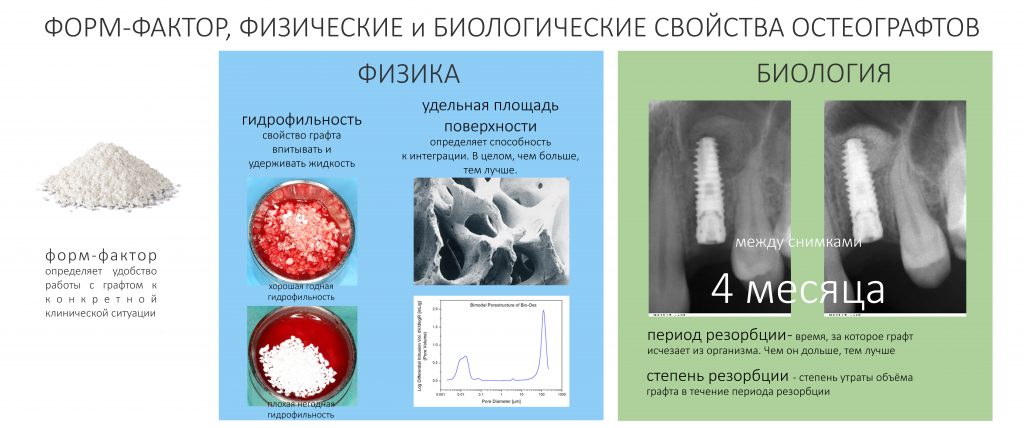
Отдельно стоит обсудить свойства графтов, выпускаемых в виде блоков или крупных фрагментов. Помимо вышеперечисленного, к ним стоит добавить прочность, упругость, хрупкость, твердость и ряд других качеств, влияющих на удобство их обработки и фиксации:

Увы, но далеко не все остеографты такого форм-фактора соответствуют этим качествам в полной мере. Выбор среди удобных в работе ксеноблоков гораздо меньше, нежели среди гранул и порошков.
Пожалуй, это все свойства остеографтов, которые нужно знать всем, докторам и пациентам. За исключением, разве что, биологических свойств, все они очень просты для понимания и могут быть изучены еще до использования в ходе остеопластической операции. Информация по составам и упаковкам остеографтов не является секретной, она есть в свободном доступе на сайтах производителей, поэтому любой желающий, при наличии интереса и базовых школьных знаний, может в них разобраться.
Несколько сложнее разобраться с назначением. Тем, для чего на самом деле нужны остеографты. Мы рассмотрим их применение при изучении конкретных методов остеопластических операций, в будущих публикациях (это, кстати, повод подписаться на обновления и добавить наш сайт в избранное). Не переключайтесь!)
Уважаемые друзья, давайте подведём некоторый итог по остеографтам.
Итак, они бывают разного происхождения, могут довольно существенно различаться по целому ряду свойств. Мы должны знать эти свойства, если хотим использовать их рационально и правильно. Вне зависимости от разницы в свойствах, правильное применение различных остеографтов всегда (или почти всегда) приводит к успешному результату остеопластической операции. Если что-то вдруг не получается — на 99,999% это проблема доктора, а не используемого биоматериала.
Задача «искусственного костного материала» — заполнить и удержать объём на время регенерации естественной кости, миграции клеток, роста сосудов и т. д. Чем медленнее остеографт резорбируется, тем дольше он удерживает пространство, тем больше времени есть у организма для восстановления утраченного участка кости. По этой причине нельзя пытаться заменить остеографт коллагеновой губкой, сушенной плазмой, тромбоцитарными соплями (PRP, FRP) и прочими гемостатическими материалами — слишком уж быстро они «исчезают» из области операции.
Ни один из существующих графтов не улучшает качество костной ткани и не ускоряет её регенерацию.
Основные ошибки при использовании остеографтов связаны, почти исключительно, с желанием затолкать его туда, где его быть, в принципе, не должно — участки острого воспаления, кисты, гранулёмы или лунки зубов мудрости. Впрочем, про это я тоже писал. Вот тут.
Вам же, уважаемые друзья, я рекомендую, найти в интернете информацию по предлагаемому вам биоматериалу и ознакомиться с ней, как минимум, на уровне понимания форм-фактора и физических свойств.
Необходимость использования остеографта в вашем случае всё равно определяет доктор, исходя из собственного опыта, клинической картины и желаемого результата.
Впрочем, это касается следующей категории биоматериалов, менее известных широкой публике, но, как ни странно, более важных. Это
Барьерные мембраны.
Я должен заметить, что это наиболее часто используемые в нашей практике биоматериалы. И вот, почему.
У остеографтов, рассмотренных в предыдущей части, простое и понятное назначение — заполнение и удержание объема. Но ведь объем мы можем заполнить чем-нибудь другим — аутокостной стружкой, костным блоком, сформировать его пластиной, сеткой, тентовыми винтами или вообще ничем не заполнять. Так уж устроен наш организм — свято место в нём пусто не бывает, и поэтому довольно скоро сформированное нами пространство для регенерации заполнится…. увы, но не желанной костной тканью.
Это происходит потому, что все ткани нашего организма регенерируют с разной скоростью.
Например, вы случайно порезали пальчик, из него даже кровь идёт.

провели гигиеническую обработку ранки — промыли, заклеили пластырем. Через сутки в ране образуется твердый тромб, затем первичный рубец — и пластырь можно снять. А еще через неделю-две, вы сможете спокойно ковырять этим пальчиком где угодно, без риска повредить новую кожу и вызвать кровотечение. Через месяц-два вы вряд ли сходу найдёте след от пореза. А через полгода — уже точно не найдёте.
Совершенно иная ситуация, если вы палец не порезали, а не дай Б-г, сломали.
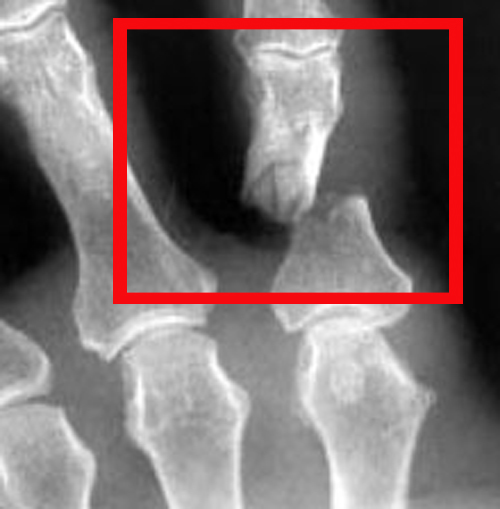
В травмпункте вам сделают снимки, репозицию (если нужно) и наложат гипс недели на три. Таким образом, палец и область перелома обездвиживаются (это необходимое условие для регенерации кости) на время заживления перелома, а более-менее внятную функциональную нагрузку, без риска осложнений,на сломанный палец можно будет дать, минимум, через месяц-полтора. Потому что костной ткани, из-за особенностей её питания и метаболизма, требуется значительно больше времени на восстановление, нежели мягким тканям.
Фактически, те же самые процессы происходят в области остеопластической операции. То пространство, которое мы только что сформировали, быстро заполнится мягкими тканями — и костной ткани уже некуда будет расти. Поэтому совершенно логичным и правильным выглядит разделение тканей с разной скоростью регенерации:
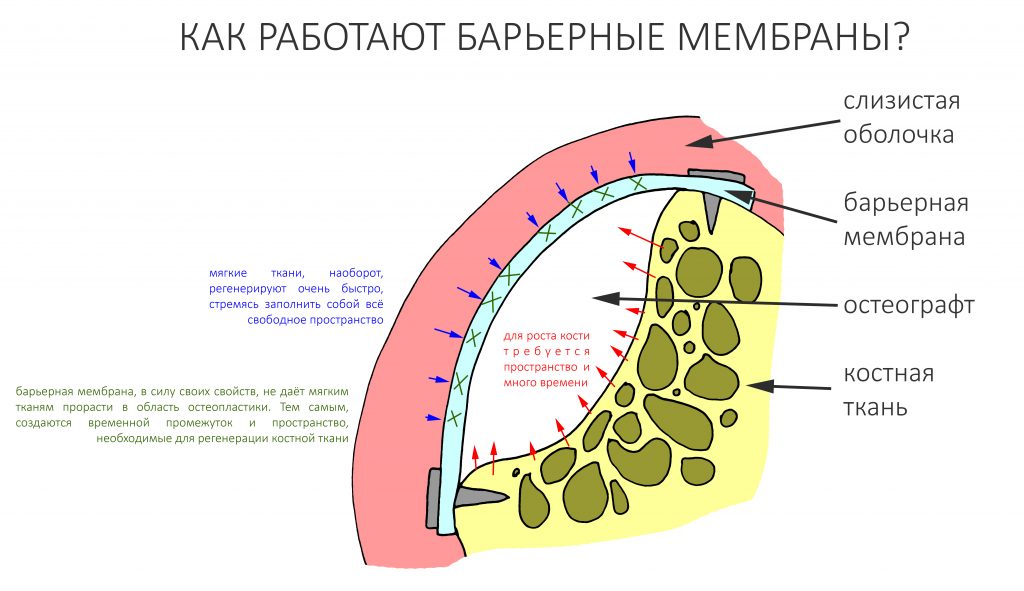
Как раз для этого и предназначены барьерные мембраны.
Виды, источники происхождения и состав
В общих чертах, все существующие барьерные мембраны можно разделить на две группы: резорбируемые и нерезорбируемые. Также существуют мембраны с очень длительным периодом резорбции и их, вроде как, пытаются выделить в отдельный класс, но на мой взгляд, их следует отнести к резорбируемым, ибо в конце концов они всё равно рассасываются и исчезают. Нерезорбируемые мембраны изготавливаются из разных биоинертных материалов (тефлон, ПТФЭ, титановые сплавы и т. д.), используются они значительно реже, про них мы поговорим, когда будем рассматривать остеопластику методом НКР.
Здесь и далее, мы будем говорить о наиболее распространенных в хирургической практике резорбируемых барьерных мембранах.
Основной компонент существующих на рынке барьерных мембран — это коллаген, органическое вещество белковой природы, главный структурный элемент соединительной ткани. Источником коллагена для барьерных мембран на 98% являются лучшие друзья и, заодно, еда человека — свинки. Изредка используется аллоколлаген (человеческого происхождения) или что-то другое (биополимеры, производные полисахаридов и т. д.).
Главная причина использования коллагена для производства барьерных мембран — это его предсказуемый распад естественным путём с помощью ферментов-коллагеназ и образованием, обычных для организма аминокислот. Без лишних продуктов распада и прочих ЛСД.
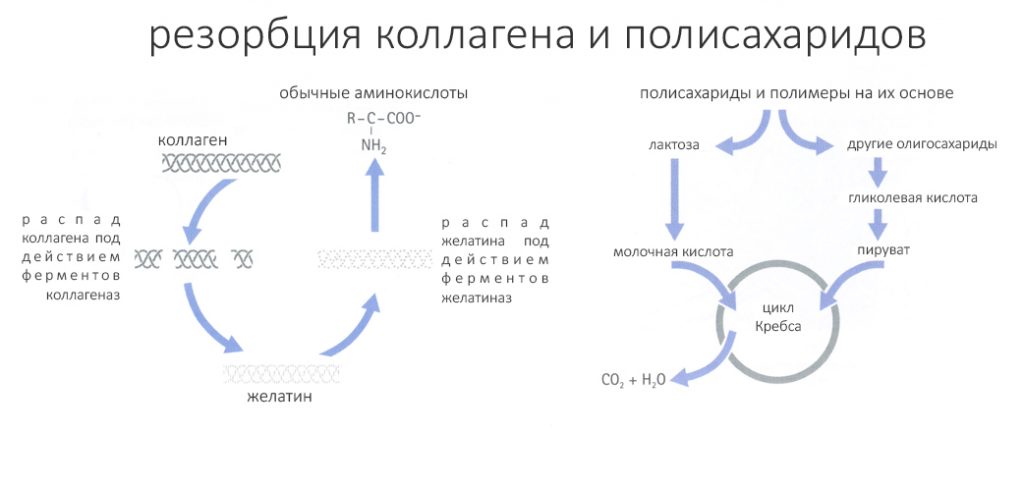
Ну, да ладно. Нас, конечных потребителей барьерных мембран, волнуют не столько секреты производства, сколько ряд критериев, важных для практики. Они, в целом, похожи на то, что мы ждём от остеографтов и биоматериалов вообще, и включают в себя:
Форм фактор.
размеры, упаковка, и т. д. Одна и та же барьерная мембрана может быть разной площади. Так, используемая нами Geistlich Bio-Gide выпускается в размерах 16х22, 25х25 и 30х40 мм

И мы выбираем нужный размер, в зависимости от масштабности хирургического вмешательства.
Физические и биологические свойства.
По аналогии с остеографтами, барьерные мембраны должны обладать рядом физических и биологических свойств.Конечно информация о свойствах важна, в первую очередь, для доктора, а не для пациента. Однако, представление о свойствах необходимо и вам, друзья, для понимания того, как мы, врачи, ориентируемся, выбирая барьерную мембрану для решения той или иной клинической задачи.

гидрофильность — ну, это само собой, ведь жидкость — это главная транспортная среда организма.
прочность — способность барьерной мембраны сохранять целостность при нагрузке и фиксации. Она не должна превращаться в лохмотья, если мы решили её забить пинами или прикрутить винтами, подлежащий графт не должен прорезываться, а натянутая мембрана — расползаться.
эластичность — барьерная мембрана должна принять форму того участка, к которому мы её адаптируем. Без лишних заломов и обработки напильником.
адгезия — идеальная барьерная мембрана, буквально, прилипает к подлежащему графту и, чаще всего, не требует какой-то специальной фиксации.
Про свойства барьерных мембран можно очень долго рассуждать. И мы однажды это сделаем, в ходе эксперимента под названием «М.П.». Вам же, друзья, нужно про свойства два момента:
— физические свойства определяют то, как ведёт себя барьерная мембрана в ходе операции. Облегчает ли она работу доктора и удешевляет ли её, или наоборот, усложняет и требует применения чего-то дополнительного. Пинов и винтов, к примеру.
— биологические свойства определяют то, что происходит с барьерной мембраной после операции. Они трудноизмеримы и, практически, неизучимы объективно. Поэтому, апеллируя к биологическим свойствам, можно «впарить» вам всё, что угодно. Именно поэтому такие критерии как «проницаемость» и «время резорбции», до сих пор являются предметов ожесточённых споров, дискуссий, драк и прочих зарубов в профессиональном стоматологическом сообществе. И, именно поэтому я призываю вас как можно меньше им верить.
А нам с вами осталось рассмотреть еще одну категорию биоматериалов:
«Искусственная слизистая оболочка» aka мукографты — новое слово в регенеративной хирургии и имплантологии.
Про мукографты, коллагеновые матрицы, предназначенные для пластики слизистой оболочки, я уже неоднократно рассказывал. Например, здесь>> и здесь>>.

В общих чертах, принцип их действия тот же, что и у упоминавшихся выше остеографтов — они заполняют место и служат каркасом для роста слизистой оболочки. К нашей сегодняшней теме, остеопластическим операциям, они прямого отношения не имеют, поэтому я не буду отнимать ваше время и расскажу про них в следующий раз, когда мы будем обсуждать пластические операции на слизистой. То есть, очень нескоро.
Вместо эпилога. Какие биоматериалы самые лучшие?
Geistlich Biomaterials, однозначно)))). Ибо RegenerationDay.
Ответ на этот вопрос и, может быть, совсем не от меня, а от Владимира Владимировича Путина более авторитетного человека хотели бы услышать не только пациенты, но и доктора-остеорегенераторы. Ибо на всех медицинских форумах, во всех профессиональных сообществах, на всех дискуссионных площадках ведутся бесконечные споры о том, что лучше и почему.
На мой взгляд, чтобы ответить на этот вопрос, его нужно, как минимум, переформулировать. Как-то так:
«Какие биоматериалы ЛУЧШЕ всего подойдут к вашей клинической ситуации?»
Ну, а далее, мы можем поискать ответ через парадигму знания их свойств.
Например, вам планируется проведение операции синуслифтинга. Это значит, нам нужен определенный объем графта, который мы можем рассчитать по определенной формуле, исходя из данных КЛКТ:
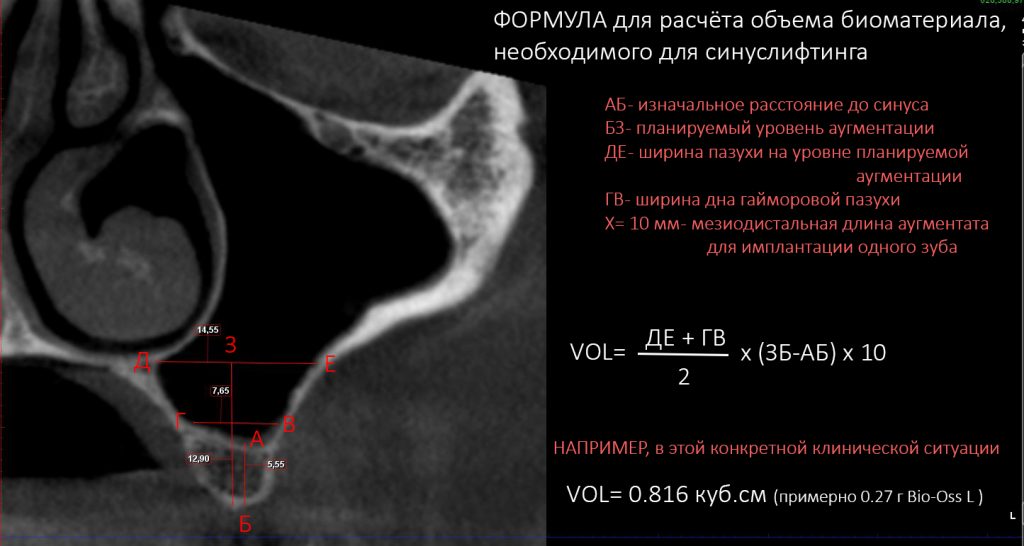
Идеально — графт в аппликаторе (удобнее), без органики (не даёт усадки), частицами крупного размера (большой объём при меньшем весе).
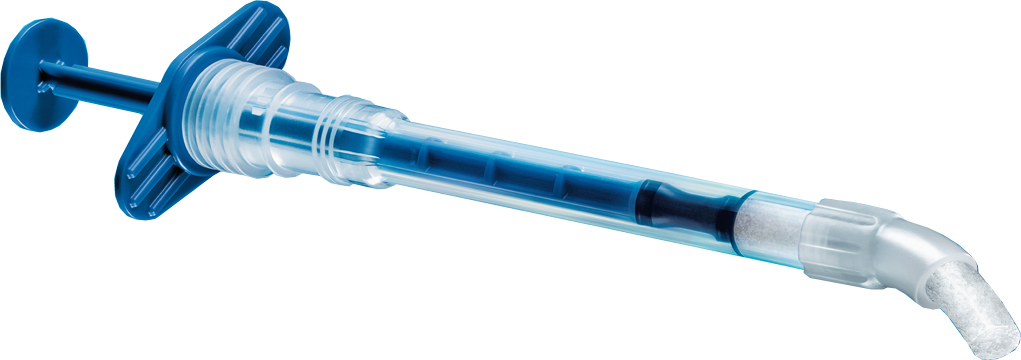
Вот этот остеографт будет самым лучшим КОНКРЕТНО ДЛЯ ВАШЕЙ ОПЕРАЦИИ. А другой остеографт в виде крупного костного блока, с содержанием коллагена не очень подойдёт. Но это не значит, что им нельзя будет получить хороший результат синуслифтинга. Просто это будет сделать сложнее.
И наоборот. При остеотомии или аугментации лунки зуба при немедленной имплантации, мы, скорее всего, намучаемся с порошком — нам нужен другой графт, другой форм-фактор и другие свойства.
Аналогичную ситуацию мы поимеем с барьерными мембранами — они бывают разных размеров (форм-фактор), различаются физическими и биологическими свойствами. И, если вам планируется направленная костная регенерация в небольшом объёме, то есть ли смысл приобретать барьерную мембрану размером 30х40 мм?

И наоборот. Планируя остеопластику, в которой барьерная мембрана сама по себе будет являться каркасом, мы уделим максимум внимания не только её размеру, но и свойствам. В частности, прочности и эластичности.
В конце концов, вы выбираете обувь и одежду по погоде и месту, автомобиль — по дорогам, где планируете ездить, женщину или мужчину по… ну, вы меня поняли. Вы делаете это рационально и всегда сможете обосновать свой выбор.
Совершенно таким же образом нужно выбирать САМЫЕ ЛУЧШИЕ БИОМАТЕРИАЛЫ конкретно для вас и вашей клинической ситуации. И никак иначе.
* * *
Завершая эту большую статью, на написание и рисование которой я потратил несколько недель, я хотел бы сказать следующее.
Уважаемые друзья. Я прекрасно понимаю, что научить пациента разбираться в биоматериалах в рамках одной статьи, этот всё равно, что небольшим техническим руководством в пятьдесят страниц, научить обычного пассажира ремонтировать самолёт. Это была заведомо невыполнимая задача, и я прекрасно отдаю себе в этом отчёт.
Но у меня была другая цель — я очень хотел, чтобы вы взглянули на используемые нами биоматериалы немного с другого ракурса.
Я хотел показать вам разницу между ними, их роль в процессе и результатах остеопластических операций.
Я хотел рассказать вам о том, как и почему мы их выбираем, когда планируем ваше лечение и чем руководствуемся, делая этот самый выбор. И, самое главное — еще раз показать, что, если мы знаем и правильно используем биоматериалы, то
результат остеопластической операции не зависит от их марки.
Уж не знаю, справился ли я с этим?
Спасибо, что дочитали до конца.
С уважением, Станислав Васильев.





Юрий
Здравствуйте,меня интересует вопрос : Что такое Аугментация кости и видно ли на ренгеновских снимках ,снимки сделаны сразу после установки имплантатов и аугментации мебранна Остеопласт?
Станислав
Юрий, добрый день. Спасибо за вопрос. Аугментация (от английского «augmentation», дополнение) — научное название остеопластических операций. То, что в народе называют «наращиванием костной ткани».
Видно ли проведённую аугментацию кости на рентгеновских снимках? Да, видно. Особенно, если сравнивать «до» и «после».
Барьерные мембраны, в т. ч. «Остеопласт» на снимках не видны. Они делаются, в основном, из органических материалов, поэтому рентгеновские лучи не задерживают.
Если будут еще вопросы — пишите или звоните. С удовольствием отвечу.
С уважением, Станислав Васильев.